|
Patente und Technologien mit interessanten Ansätzen und teilweise interessanten Berechnungen und Beschreibungen
Patent Recherche 2 : Öl Kohlenwassertoffe Treibstoff aus CO2 und elektrichen Strom
1
|
|
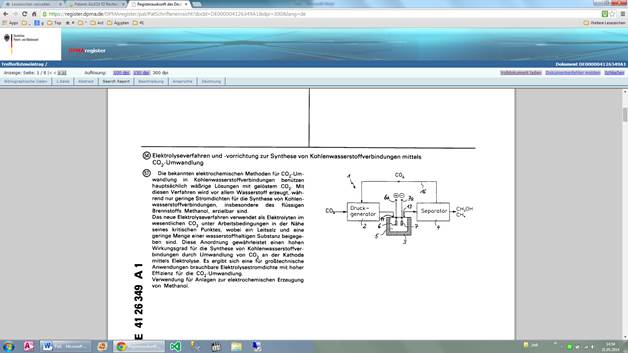
Elektrolyseverfahren und -vorrichtung zursynthesevon kohlenwasserstoffverbindungen mittelsco(pfeil abwaerts)2(pfeil abwaerts)-umwandlung
Bandi (ehemals Solar-fuel , ZSW)
1991
DE 4126349 A1
https://register.dpma.de/DPMAregister/pat/PatSchrifteneinsicht?docId=DE000004126349A1&page=1&dpi=300&lang=de
Elektrolyseverfahren zurSynthesevon Kohlenwasser stoffverbindungen, insbesondere flüssigen Brennstoffen wie Methanol, mittels Umwandlung von im Elektrolyten enthaltenen Kohlendioxid (CO2) an der Kathode,
dadurch gekennzeichnet,
daß der Elektrolyt im wesentlichen ausCO2, einem beigegebenen Leitsalz und einer beigegebenen wasserstoffhaltigen Substanz besteht, und daß während der Elektrolyse Druck und Temperatur des Elektrolyten wenigstens annähernd so hoch wie die seinem kritischen Punkt entsprechenden Werte gehalten werden.
2. Elektrolyseverfahren nach Anspruch 1, dadurch gekenn zeichnet, daß als wasserstoffhaltige Substanz Wasser (H2O), Chlorwasserstoff (HCl) oder Schwefelwasserstoff (H2S) bei gegeben wird.
|
2
|
|
Methanol-Synthese-Verfahren
DE 112010002562 T5
Johnson 2010
Es wird ein Methanol-Synthese-Verfahren beschrieben, das die Umsetzung eines Prozessgases, das Wasserstoff, Kohlendioxid und Kohlenmonoxid enthält, über einem Katalysator umfasst, der geformte Einheiten umfasst, die aus einem reduzierten und passivierten Katalysatorpulver geformt wurden, wobei das Pulver Kupfer im Bereich von 10–80 Gew.-%, Zinkoxid im Bereich von 20–90 Gew.-%, Aluminiumoxid im Bereich von 5–60 Gew.-% sowie ggf. eine oder mehrere oxidische Promotorenverbindungen, die ausgewählt sind aus Verbindungen von Mg, Cr, Mn, V, Ti, Zr, Ta, Mo, W, Si und Seltenen Erden, im Bereich von 0,01–10 Gew.-% umfasst, um ein Produktgas zu bilden, und Kondensieren von Methanol, Wasser und Oxygenat-Nebenprodukt daraus, wobei der Anteil an gesamtem Oxygenat-Nebenprodukt im Kondensat unterhalb 500 ppm liegt.
. Diese Reaktionen werden nachfolgend dargestellt:CO+ 2H2→ CH3OHCO2+ 3H2→ CH3OH + H2O
|
3
|
|
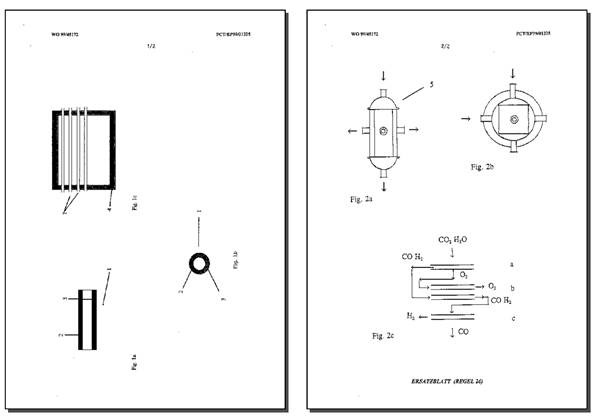
Synthesis gas produced by electrolysis using hollow micro-fibers as solid electrolytes
DE 19908863 A1
Rennebeck 1998DE 19908863 A1
Synthesis gas is obtained by electrolysis using hollow micro-fibers as solid electrolytes, the internal and external surfaces of which support the anodes and cathodes. The fibers are made using zirconium oxide stabilized by yttrium. The external diameter is from 50 to 280 mu m. The feed gas is a mixture ofCO2and H2O which following high temperature electrolysis is converted toCOandH2, the O2 separating through the fiber wall as a permeate. The hydrogen is subsequently separated using a gas separation membrane also made of hollow micro-fibers.
Sieht super aus.. Umsetzung fehlt
|
4
|
|
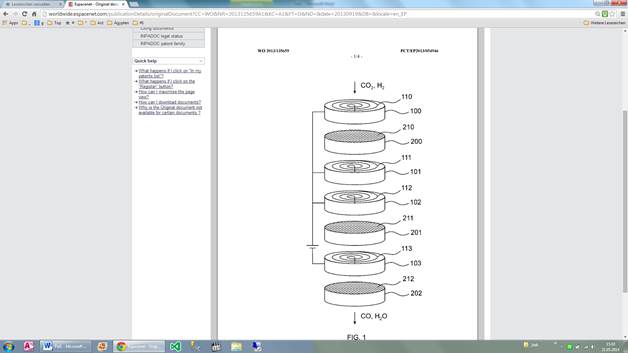
Verfahren zur reduktion von kohlendioxid bei hohen temperaturen an oxidischen katalysatoren umfassend nickel und ruthenium
WO 2013135659 A1
Bayer 2012WO 2013135659 A1
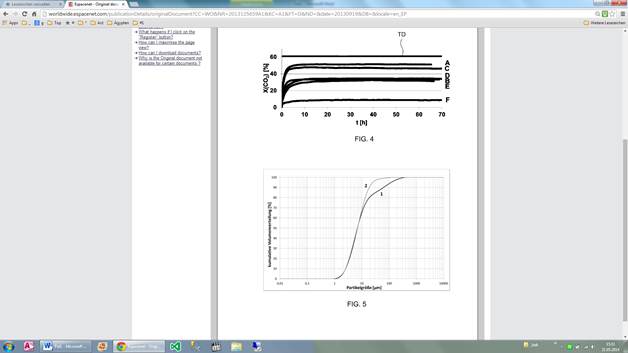
Ein Verfahren zur Reduktion von Kohlendioxid, umfassend den Schritt der Reaktion von Kohlendioxid und Wasserstoff in Gegenwart eines Katalysators unter Bildung von Kohlenmonoxid und Wasser, ist dadurch gekennzeichnet, dass die Reaktion bei einer Temperatur von ≥ 700 °C durchgeführt wird und dass der Katalysator ein oxidischer Katalysator ist, der Ni und Ru umfass
Verfahren zur Reduktion von Kohlendioxid bei hohen Temperaturen an oxidischen Katalysatoren umfassend Nickel und Ruthenium
Die vorliegende Erfindung betrifft ein Verfahren zur Reduktion von Kohlendioxid, umfassend den Schritt der Reaktion von Kohlendioxid und Wasserstoff in Gegenwart eines Katalysators unter Bildung von Kohlenmonoxid und Wasser. Die Erfindung betrifft weiterhin die Verwendung eines solchen Katalysators in der Reduktion von Kohlendioxid.
Die sogenannte Wassergas-Verschiebungsreaktion (water gas shift reaction, WGS) wird seit Langem zur Verringerung des CO-Anteils in Synthesegas eingesetzt und beinhaltet die Reaktion von Kohlenmonoxid mit Wasser unter Bildung von Kohlendioxid und Wasserstoff. Diese Reaktion ist eine Gleichgewichtsreaktion.
|
5
|
|
Method for controlling, generation of synthesis gas containing carbon monoxide and free hydrogen by steam reformer, involves feeding hydrocarbons, free hydrogen, carbon dioxide, carbon monoxide and steam to steam reformer stage
DE 102006050057 A1
Linde 2006
DE 102006050057 A1
https://register.dpma.de/DPMAregister/pat/PatSchrifteneinsicht?docId=DE102006050057A1
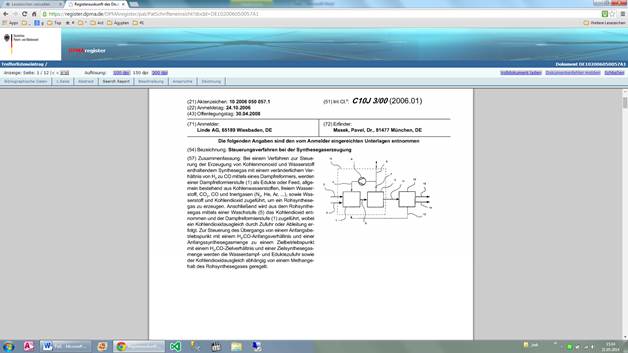
The method involves feeding hydrocarbons, free hydrogen, carbon dioxide, carbon monoxide, inert gases and steam to a steam reformer stage (1) to generate crude synthesis gas. The carbon dioxide is taken off from the crude synthesis gas by a scrubbing stage (5). The steam, feed and a carbon dioxide equilibration performed by feed are controlled as a function of methane content of the crude synthesis gas for control of the transfer from a starting operating point having a starting hydrogen-carbon monoxide ratio to a target operating point having a target hydrogen-carbon monoxide ratio.
|
6
|
|
Method for optimizing thermal synthesis of carbon, involves introducing finely divided carbon into gas-tight or hydrogen-dense heated rotary furnace so that carbon is heated with water to produce carbon monoxide and hydrogen
DE 102010036144 A1
Brück, 2010
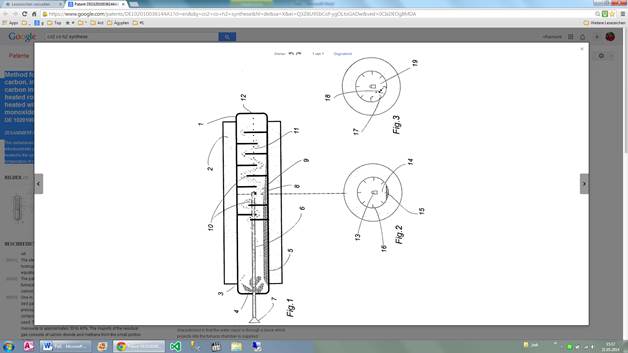
The carbonaceous material or finely divided carbon (4) or form of dust is introduced into gas-tight or hydrogen-dense heated rotary furnace and is heated to the synthesis temperature, so that carbon is heated with water to produce carbon monoxide and hydrogen. The water vapor is supplied only when the temperature of carbon is about 800 [deg] C. An independent claim is included for device for optimizing thermal synthesis of carbon.
The steam reforming is a well known process for the production of hydrogen.They are normally here from methane.The corresponding equation is: CH4 + H2O =>CO+ 3H2.
|
7
|
|
Verfahren zur Erzeugung von Gasprodukten aus Synthesegas
DE 102011016789 A1
Linde 2011
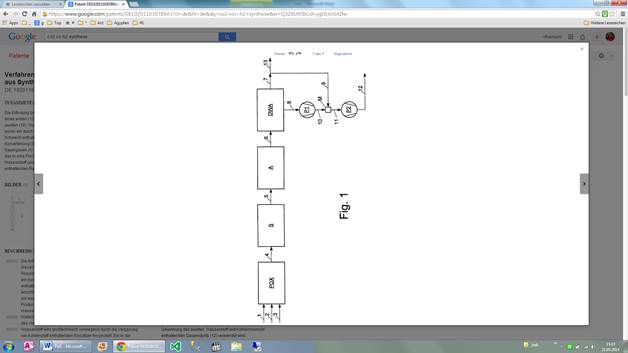
Die Erfindung betrifft ein Verfahren sowie eine Vorrichtung zur Gewinnung eines ersten (13), im Wesentlichen aus Wasserstoff bestehenden, und eines zweiten (12), Wasserstoff und Kohlenmonoxid enthaltenden Gasproduktes, wobei ein durch Partielle Oxidation (POX) aus einem Kohle und/oder Schweröl enthaltenden Einsatz (3) erzeugtes Synthesegas (4) durch Konvertierung (S), anschließende Trocknung und die Entfernung von Sauergasen (A) in ein wasserstoffreiches Gasgemisch (6) umgesetzt wird, das in eine Produktreinheit aufweisende Wasserstofffraktion (7) sowie ein Wasserstoff und Kohlenmonoxid enthaltendes Restgas (8) zerlegt wird. Erfindungsgemäß wird zumindest ein Teil (10) des Wasserstoff und Kohlenmonoxid enthaltenden Restgases (8) zur Gewinnung des zweiten, Wasserstoff und Kohlenmonoxid enthaltenden Gasprodukts (12) verwendet.
Ein Beispiel für ein Oxogas ist Methanol-Synthesegas, das aus Wasserstoff (H2), Kohlenmonoxid (CO) und Kohlendioxid (CO2) besteht, wobei seine Stöchiometriezahl S, die sich aus den molaren Konzentrationen [H2], [CO] und [CO2] seiner Bestandteile gemäß S = ([H2] – [CO2])/([CO] + [CO2]) errechnet, einen Wert von ca. 2 besitzt.
->indirekt
|
8
|
|
Method for reducing carbon dioxide at high temperatures on catalysts especially carbide supported catalysts
WO 2013135673 A1
Bayer 2012
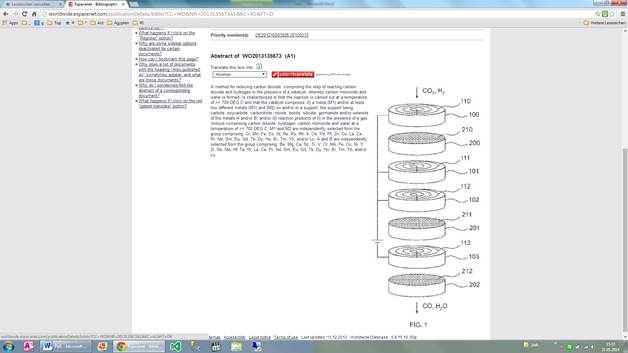
A method for reducing carbon dioxide, comprising the step of reacting carbon dioxide and hydrogen in the presence of a catalyst, whereby carbon monoxide and water is formed, is characterized in that the reaction is carried out at a temperature of ≥ 700 °C and that the catalyst comprises: (I) a metal (M1) and/or at least two different metals (M1) and (M2) on and/or in a support, the support being carbide
->CO2 an Mox
|
9
|
|
Verfahren zur abwechselnden Erzeugung oder Speicherung elektrischer Energie durch chemische Umwandlung von Kohlenstoff
DE 102012021256 A1
Karl Werner Dietrich 2012 Bayer
Als wirtschaftliche Alternative zur Nutzung überschüssiger erneuerbarer Energien wurden traditionelle Reaktionen aus der Kohlechemie erkannt. So reagiert Kohle mit Wasser (Kohlenstoff und Wasser in Molverhältnis 1:1/Reaktionsgleichung 1) unter Druck und Hitze zu Kohlenmonoxid und Wasserstoff Das äquimolare Gasgemisch aus Wasserstoff und Kohlenmonoxid wird im folgenden ”Synthesegas” genannt. Fügt man zum Synthesegas weitere 2 Mol Wasserstoff zu, durch Wasserelektrolyse aus Wind- oder Solarstrom gewonnen (Reaktionsgleichung 3), so entsteht in einer nach dem Chemiker ”Sabatier” genannten Reaktion Methan und Wasser im Molverhältnis 1:1 (Reaktionsgleichung 2).Reaktionsgleichung 1.) C + H2O =CO+H2Reaktionsgleichung 2.) (CO+H2) + 2H2 = CH4 + H2OReaktionsgleichung 3.) 2H2O = 2H2 + O2
->zu global
|
10
|
|
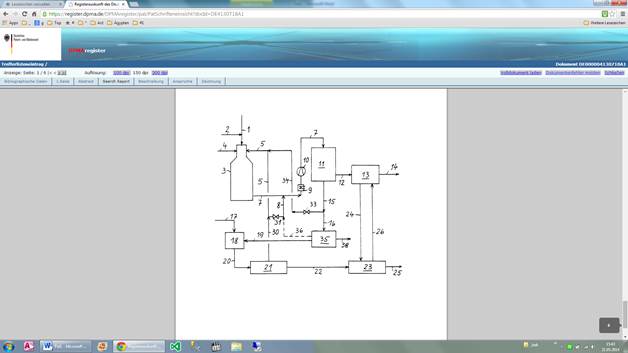
Verfahren zur erzeugung eins synthesegases fuer die methanolsynthese
DE 4130718 A1
Metallgesellschaft AG 1991
Verfahren zur Erzeugung eines Synthesegases für die Methanolsynthese und Umsetzen des Synthesegases an einem Katalysator zu einem methanolreichen Produktstrom, wobei man ein methanhaltiges Kohlenwasserstoffgas mit Sauerstoff und Wasserdampf in einem Reformierreaktor katalytisch autotherm bei Temperaturen am Reaktoraustritt von 800 bis 1300°C und einem Druck von 10 bis 100 bar umsetzt und aus dem Reformierreaktor ein rohes Synthesegas abzieht, dessen Komponenten vor allem Wasserstoff, Kohlenmonoxid und Kohlendioxid sind,
dadurch gekennzeichnet,
daß man in den Reformierreaktor zur katalytisch autothermen Umsetzung ein wasserstoffreiches Gas einleitet, das freien Wasserstoff enthält, und daß man ohne Entfernung von Kohlendioxid ein für die Methanolsynthese geeignetes Synthesegas erzeugt, in welchem die Konzentrationen der Komponenten H2,COundCO2ein als Stöchiometriezahl bezeichnetes molares Verhältnis (H2-CO2) : (CO+CO2) von 1,97 bis 2,2 ergeben.
|
11
|
|
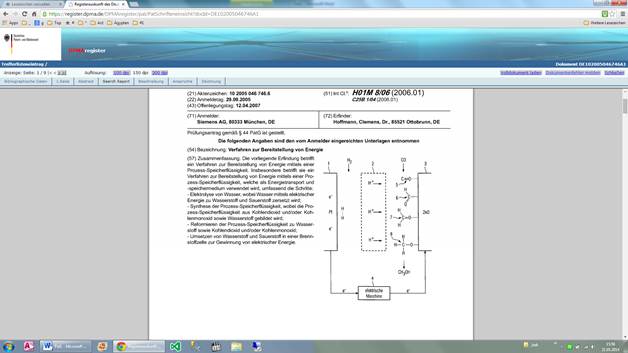
Generation of energy in the form of methanol in a synthesising process using electrolysis of water
DE 102005046746 A1
Siemens AG 2005
The synthesis of methanol usingH2andCO2has disassociated hydrogen on a plate anode [1]. The protons wander through the exchange membrane [2] in the direction of a ZnO cathode [3]. The combination of electrons ands protons results in a methoxy species [8] that sets methanol free from the cathode surface.
https://register.dpma.de/DPMAregister/pat/PatSchrifteneinsicht?docId=DE102005046746A1
|
|
|
|
|
.
|